Патогенетические факторы ишемической кардиомиопатии: результаты многомерного факторного анализ
Pathogenetic factors of ischaemic cardiomyopathy: results of multivariate factor analysis- DOI
- 10.0.23.34/ATB-2025-1-1-6
- Страницы / Pages
- 74-90
Аннотация
Актуальность. Патогенез ишемической кардиомиопатии (ИКМП) до конца не изучен.
Цель. Выявление ключевых патогенетических факторов развития ИКМП с помощью многофакторного анализа и определение степени их влияния на заболевание.
Материал и методы. В исследование включено 60 больных ишемической болезнью сердца (ИБС) с ИКМП, 44 больных ИБС без кардиомиопатии. Материалом служили кровь и костный мозг, в которых определяли содержание десквамированных эндотелиальных клеток (ДЭК), классических, промежуточных, неклассических, переходных моноцитов, ранних и поздних эндотелиальных прогениторных клеток (ЭПК) методом проточной цитофлуориметрии. В плазме крови и надосадке костного мозга оценивали концентрацию VEGF-А, SDF-1, МСР-1, M-CSF, GM-CSF, TNF-α, HIF-1α, IL-6, IL-10, IL-13, IFN-γ методом иммунофлуоресцентного и иммуноферментного анализа. Выполнен корреляционный и многомерный факторный анализ при р < 0,05.
Результаты. На уровне крови первый по степени влияния на ИКМП фактор сочетал в себе содержание SDF-1, HIF-1α, M-CSF, ДЭК (обусловливал 41,8% дисперсии), второй — IL-10 и МСР-1 (31,1%), третий — поздних ЭПК (26,3%), четвертый — IL-6 и IL-13 (21,6%). В костном мозге первый по значимости фактор объединял содержание IL-10, IFN-γ, IL-13, M-CSF/IL-13 и классических моноцитов (47,1%), второй — неклассических моноцитов и TNF-α (35,2%), третий — VEGF-A, МСР-1, GM-CSF, HIF-1α (32,7%), четвертый — ранних ЭПК и IL-6 (25,5%). В костном мозге у больных ИБС без кардиомиопатии установлена связь между концентрацией IL-6 и SDF-1 (r= – 0,781, p = 0,013); у пациентов с ИКМП — IL-6 и MCP-1 (r = 0,899, p = 0,014).
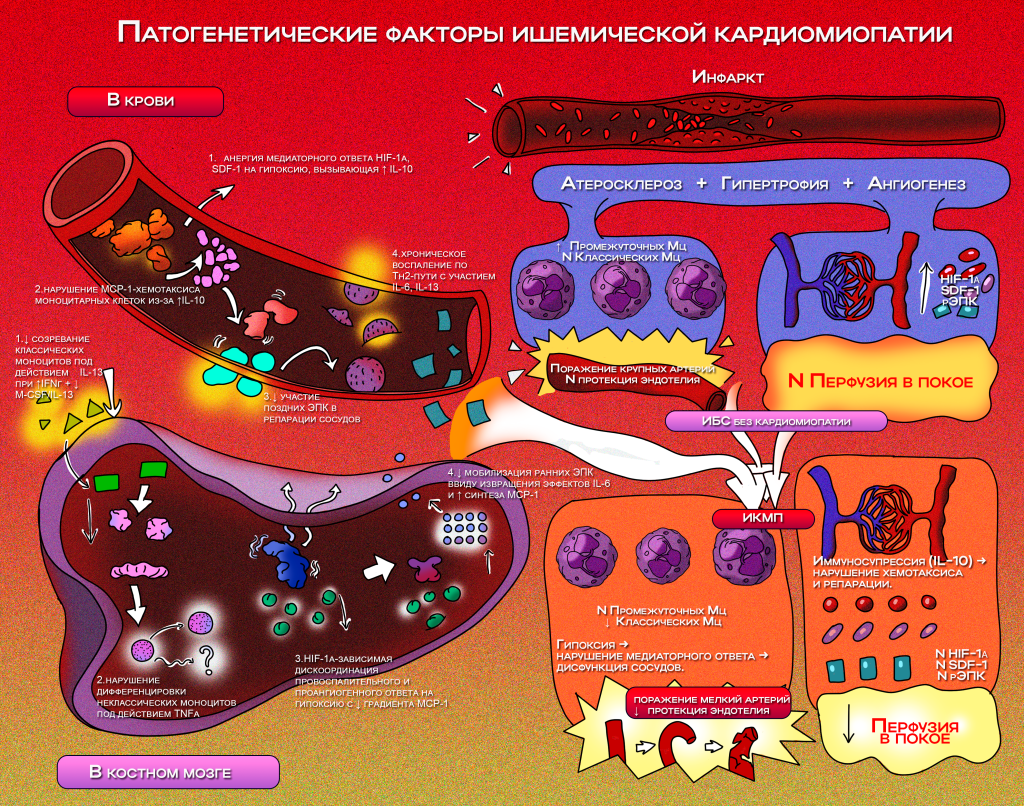
Заключение. Ведущими патогенетическими факторами ИКМП являются: в крови — анергия медиаторного ответа HIF-1α, SDF-1 на гипоксию с гиперпродукцией IL-10; в костном мозге — недостаточность классических моноцитов и соотношения M-CSF/IL-13 в условиях избытка IFN-γ.
Abstract
Background. The pathogenesis of ischemic cardiomyopathy (ICM) is not fully understood. Aim. This study aims to identify key pathogenetic factors involved in the development of ICMP through multifactorial analysis and to determine the extent of their contribution to disease progression. Material and methods. The study included 60 patients with coronary heart disease (CHD) and ICMP, and 44 patients with CHD without evidence of cardiomyopathy.Blood and bone marrow samples were analysed by flow cytometry to assess the content of desquamated endothelial cells (DEC); classical, intermediate, non-classical, transitional monocytes; and early and late endothelial progenitor cells (EPC). In plasma and bone marrow supernatant, the concentrations of VEGF-A, SDF-1, MCP-1, M-CSF, GM-CSF, TNF-α, HIF-1α, IL-6, IL-10, IL-13, and IFN-γ were assessed using immunofluorescence and enzyme-linked immunosorbent assay. Correlation and multivariate factor analysis were performed at p < 0.05. Results. At the blood level, the primary factor terms of influence on ICMP was the concentrations of SDF-1, HIF-1α, M-CSF and DEC, accounting for 41.8% of the total variance. The second most influential factor was the concentration of IL-10 and MCP-1 (31.1%); the third was the content of late endothelial progenitor cells (EPCs) (26.3%); and the fourth, the levels of IL-6 and IL-13 (21.6%). In the bone marrow, the most significant factor was the concentrations of IL-10, IFN-γ, IL-13, M-CSF/IL-13, and classical monocytes (47.1%). The second factor involved non-classical monocytes and TNF-α (35.2%); the third, VEGF-A, MCP-1, GM-CSF, and HIF-1α (32.7%); and the fourth, early EPC and IL-6 (25.5%). In the bone marrow of patients with CHD without cardiomyopathy, a significant negative correlation was observed between IL-6 and SDF-1 concentrations (r = – 0.781, p = 0.013), while in patients with ICMP, a strong positive correlation was found between IL-6 and MCP-1 (r = 0.899, p = 0.014). Conclusions. Pathogenetic factors contributing to the development of ICMP were identified. In the blood, the most significant was an anergic mediator response of HIF-1α and SDF-1 to hypoxia with hyperproduction of IL-10. In the bone marrow, deficiency of classical monocytes and the ratio of M-CSF/IL-13 under conditions of excess IFN-γ.
Список литературы
1. Cabac-Pogorevici I., Muk B., Rustamova Y., Kalogeropoulos A., Tzeis S., Vardas P. Ischaemic cardiomyopathy. Pathophysiological insights, diagnostic management and the roles of revascularisation and device treatment. Gaps and dilemmas in the era of advanced technology. Eur. J. Heart Fail. 2020, 22(5), 789–799, DOI: 10.1002/ejhf.1747.
2. Liga R., Colli A., Taggart D. P., Boden W. E., De Caterina R. Myocardial Revascularization in Patients With Ischemic Cardiomyopathy: For Whom and How. J. Am. Heart Assoc. 2023, 12(6), e026943, DOI: 10.1161/JAHA.122.026943.
3. Pastena P., Frye J. T., Ho C., Goldschmidt M. E., Kalogeropoulos A. P. Ischemic cardiomyopathy: epidemiology, pathophysiology, outcomes, and therapeutic options. Heart Fail. Rev. 2024, 1, 287–299, DOI: 10.1007/s10741-023-10377-4.
4. Стельмашенко А. И., Беляева С. А., Карпов Р. М., Андреев С. Л. Оценка состояния экстрацеллюлярного матрикса миокарда у пациентов с ишемической кардиомиопатией. Морфологический альманах имени В. Г. Ковешникова. 2021, 4, 65–71.
5. Ungvari Z., Tarantini S., Kiss T., Wren J. D., Giles C. B., Griffin C. T., et al. Endothelial dysfunction and angiogenesis impairment in the ageing vasculature. Nat. Rev. Cardiol. 2018, 15(9), 555–565, DOI: 10.1038/s41569-018-0030-z.
6. Zhang J. Biomarkers of endothelial activation and dysfunction in cardiovascular diseases. Rev. Cardiovasc. Med. 2022, 23(2), 73, DOI: 10.31083/j.rcm2302073.
7. Urazova O., Chumakova S., Vins M., Maynagasheva E., Shipulin V., Pryahin A., et al. Characteristics of humoral regulation of differentiation of bone marrow monocyte subpopulations in patients with ischemic cardiomyopathy. Int. J. Biomed. 2019, 9(2), 91–96, DOI:10.21103/Article9(2)_OA1.
8. Chumakova S., Urazova O., Vins M., Kolobovnikova Y., Churina E., Novitskiy V., et al. Galectin 3 and non-classical monocytes of blood as myocardial remodeling factors at ischemic cardiomyopathy. Int. J. Cardiol. Heart Vasc. 2021, 33, 100766, DOI: 10.1016/j.ijcha.2021.100766 .
9. Денисенко О. А., Чумакова С. П., Уразова О. И., Шипулин В. М., Пряхин А. С. Цитокины и HIF-1α как факторы дисрегуляции миграции и дифференцировки моноцитарных клеток-предшественниц эндотелиоцитов в патогенезе ишемической кардиомиопатии. Acta Biomedica Scientifica. 2022, 7(5-2), 21–30, DOI: 10.29413/ABS.2022-7.5-2.3
10. Чумакова С. П., Уразова О. И., Денисенко О. А., Винс М. В., Шипулин В. М., Пряхин А. С., et al. Цитокины в механизмах регуляции моноцитопоэза при ишемической болезни сердца. Гематология и трансфузиология. 2022, 67(4), 511–524, DOI: 10.35754/0234-5730-2022-67-4-511-524.
11. Чумакова С. П., Уразова О. И., Шипулин В. М., Денисенко О. А., Гладковская М. В., Андреев С. Л., и др. Роль медиаторов ангиогенеза в мобилизации ранних и поздних эндотелиальных прогениторных клеток из костного мозга при ишемической болезни сердца. Вестник Российской академии медицинских наук. 2023, 78(6), 549–559, DOI: 10.15690/vramn12452.
12. Чумакова С. П., Денисенко О. А., Уразова О. И., Шипулин В. М., Андреев С. Л., Винс М. В., и др. Роль МСР-1 и SDF-1 в нарушении мобилизации эндотелиальных прогениторных клеток из костного мозга при ишемической болезни сердца. Медицинская иммунология. 2024, 26(5), 1053–1060, DOI: 10.15789/1563-0625-TRO-16762.
13. Chumakova S. P., Urazova O. I., Shipulin V. M., Andreev S. L., Denisenko O. A., Gladkovskaya M. V., et al. Role of angiopoetic coronary entothelial dysfunction in the pathogenesis of ischemic cardiomyopahy. Biomedicines. 2023, 11(7), 1950, DOI: 10.3390/biomedicines11071950.
14. Петри А., Сэбин К. Наглядная Медицинская статистика: перевод с англ.; под ред. В. П. Леонова. – 4-е изд., перераб. и доп. ГОЭТАР-Медиа: Москва. 2021, 232, DOI: 10.33029/9704-5904-1-2021-NMS-1-232.
15. Овсянников Г. Н. Факторный анализ в доступном изложении: Изучение многопараметрических систем и процессов. Издательство «Ленанд»: Москва. 2022, 176, ISBN: 9785951932112.
16. Felker G. M., Shaw L. K., O’Connor C. M. A standardized definition of ischemic cardiomyopathy for use in clinical research. J. Am. Coll. Cardiol. 2002, 39(2), 210–218, DOI: 10.1016/s0735-1097(01)01738-7.
17. Sato Т., Takeda N. The roles of HIF-1α signaling in cardiovascular diseases. J. Cardiol. 2023, 81(2), 202–208, DOI: 10.1016/j.jjcc.2022.09.002.
18. Ushach I., Zlotnik A. Biological role of granulocyte macrophage colony-stimulating factor (GM-CSF) and macrophage colony-stimulating factor (M-CSF) on cells of the myeloid lineage. J. Leukoc. Biol. 2016, 100(3), 481–489, DOI: 10.1189/jlb.3RU0316-144R.
19. Jiang Q., Huang K., Lu F., Deng S., Yang Z., Hu S. Modifying strategies for SDF-1/CXCR4 interaction during mesenchymal stem cell transplantation. Gen. Thorac. Cardiovasc. Surg. 2022, 70(1), 1–10, DOI: 10.1007/s11748-021-01696-0.
20. Feng Y., Ye D., Wang Z., Pan H., Lu X., Wang M., et al. The Role of Interleukin-6 Family Members in Cardiovascular Diseases. Front. Cardiovasc. Med. 2022, 9, 818890, DOI: 10.3389/fcvm.2022.818890.
21. Castro C. A., Buzinari T. C., Lino R. L. B., Araújo H. S. S., Aníbal F. F., Verzola R. M. M., et al. Profile of IL-6 and TNF in Foam Cell Formation: An Improved Method Using Fluorescein Isothiocyanate (FITC) Probe [Article in Portuguese, English]. Arq. Bras. Cardiol. 2022, 119(4), 533–541, DOI: 10.36660/abc.20210682.
22. Wang X., Wong K., Ouyang W., Rutz S. Targeting IL-10 Family Cytokines for the Treatment of Human Diseases. Cold Spring Harb. Perspect. Biol. 2019, 11(2), a028548, DOI: 10.1101/cshperspect.a028548.
23. Proto J. D., Doran A. C., Gusarova G. A., Yurdagul A., Sozen E., Subramanian M., et al. Regulatory T Cells Promote Macrophage Efferocytosis during Inflammation Resolution. Immunity. 2018, 49, 1–12, DOI: 10.1016/j.immuni.2018.07.015.
24. Tian M., Yuan Y. C., Li J. Y., Gionfriddo M. R., Huang R. C. Tumor necrosis factor-α and its role as a mediator in myocardial infarction: A brief review. Chronic Dis. Transl. Med. 2015, 1(1), 18–26, DOI: 10.1016/j.cdtm.2015.02.002.
25. Singh S., Anshita D., Ravichandiran V. MCP-1: Function, regulation, and involvement in disease. Int. Immunopharmacol. 2021, 101, Part B, 107598, DOI: 10.1016/j.intimp.2021.107598.
26. Teh Y. C., Ding J. L., Ng L. G., Chong S. Z. Capturing the fantastic voyage of monocytes through time and space. Front. Immunol. 2019, 10, 834. DOI: 10.3389/fimmu.2019.00834.
27. Chopra H., Hung M. K., Kwong D. L. W., Zhang C. F., Pow E. H. N. Insights into endothelial progenitor cells: origin, classification, potentials, and prospects. Stem Cells Intl. 2018, 2018, 9847015, DOI: https://doi.org/10.1155/2018/9847015.
28. Денисенко О. А., Чумакова С. П., Уразова О. И. Эндотелиальные прогениторные клетки: происхождение и роль в ангиогенезе при сердечно-сосудистой патологии. Сибирский журнал клинической и экспериментальной медицины. 2021, 36(2), 23–29, DOI: 10.29001/2073-8552-2021-36-2-23-29.
29. Martín-Bórnez M., Falcón D., Morrugares R., Siegfried G., Khatib A. M., Rosado J. A., et al. New Insights into the Reparative Angiogenesis after Myocardial Infarction. Int. J. Mol. Sci. 2023, 24(15), 12298, DOI: 10.3390/ijms241512298.