Как сделать данные находимыми, доступными, взаимно совместимыми, переиспользуемыми, а также эмерджентными (FAIRE): Предложения по использованию модельно-ориентированной интеграции данных (SOMEDAI) в системно-биологической подготовке к следующим эпидемиям
Making data Findable, Accessible, Interoperable, Reusable and Emergeable (FAIRE): Proposing a Silicon Organism Model-Engrossed Data Integration (SOMEDAI) approach in Systems Biological preparations for the next epidemics- DOI
- 10.0.23.34/ATB-2025-1-1-4
- Страницы / Pages
- 51-64
Аннотация
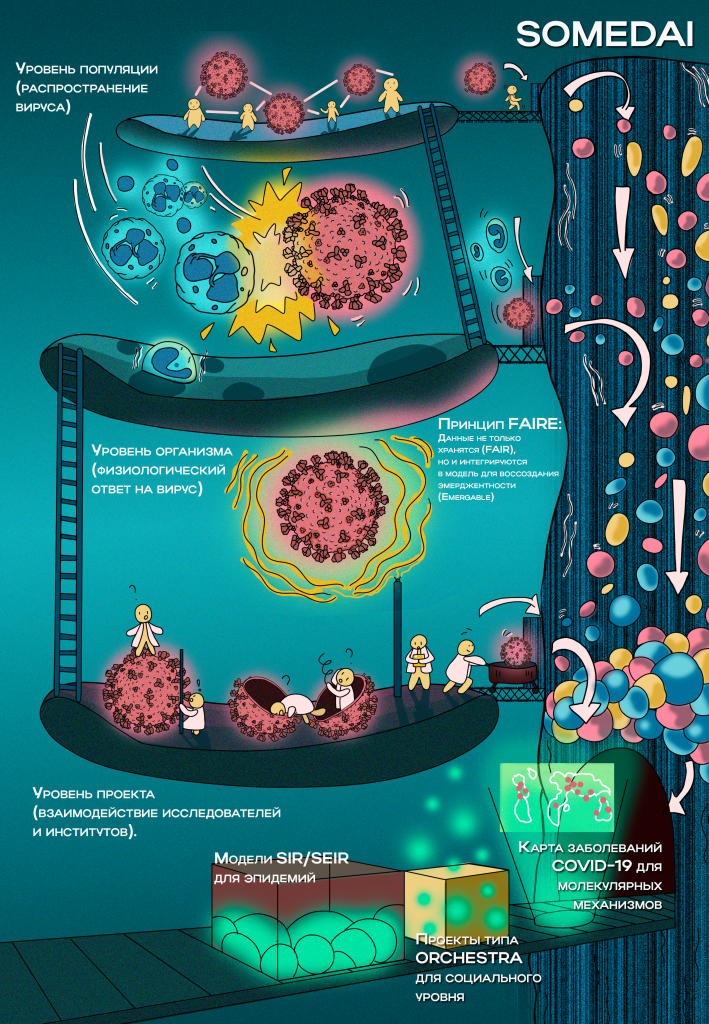
Настоящая работа посвящена обсуждению концепции эмерджентности в современной системной биологии и затрагивает применение этой концепции в эпидемиологическом моделировании COVID-19, где можно выделить три направления эмерджентности: (i) эмерджентность эпидемии в популяции, возникающая из взаимодействий между неинфицированными, инфицированными, и переболевшими индивидуумами; (ii) эмерджентность физиологического ответа на инфекцию на уровне инфицированного организма, возникающая из взаимодействий между биомолекулами, и (iii) эмерджентность самого научно-исследовательского проекта возникающая из взаимодействий между различными институтами и частниками проекта.
Системно-биологическое понимание биологической эмерджентности вызывает необходимость некоторых изменений в подходах по дата менеджменту. С добавление концепции эмерджентости, классический подход так называемого FAIR дата менеджмента (аббревиация от Findable, Accessible, Interoperable, Reusable), трансформируется в FAIRE (Findable, Accessible, Interoperable, Reusable, Emergeable), то есть данные становятся не только легко находимыми, доступными, взаимно совместимыми, но также эмерджентными. Для реализации FAIRE дата менеджмента предлагается подход модельно-ориентированной интеграции данных (SOMEDAI), при котором данные не просто сохраняются в базах данных, но сразу же интегрируются в математическую модель, что позволяет одновременно верифицировать качество данных и реконструировать биологическую эмерджентность.
Abstract
This manuscript is dedicated to the concept of emergence in modern systems biology and discusses the essence of this concept, its role, and its implementation using the example of epidemic modeling for COVID-19, where three dimensions of emergence should be integrated: (i) the emergence of the epidemic and the spread of the virus in a population from interactions between susceptible, infected, and recovered individuals; (ii) the emergence of health-related properties of one individual from interactions between biomolecules; (iii) the emergence of the research project from interactions between various institutions collecting different pieces of clinical data. Systems biological understanding of biological emergence may require changes in data management approaches. By adding the concept of Emergence, classical FAIR data management may be extended to FAIRE, where data become not only Findable, Accessible, Interoperable, and Reusable, but also Emergeable (FAIRE). To implement FAIRE data management, we propose a Silicon Organism Model-Engrossed Data Integration approach (SOMEDAI), where data are not just stored in separate databases, but are integrated into a mathematical model. The latter allows for validating data consistency and using the data to reconstruct the emergent behaviour of the whole system.
Список литературы
- Alberghina L., Westerhoff H. V. Systems Biology: Definitions and Perspectives. Springer: Berlin, Germany. 2005.
- Westerhoff H. V., Kolodkin A. N., Conradie R., Wilkinson SJ., Bruggeman F. J., Krab K., et al. Systems biology towards life in silico: mathematics of the control of living cells. J. Math. Biol. 2009, 58(1-2), 7—34, DOI: 10.1007/s00285-008-0160-8.
- Stephan A. The dual role of ‘emergence’ in the philosophy of mind and in cognitive science. Synthese. 2006, 151(3), 485—498, DOI: 10.1007/s11229-006-9019-y.
- Kolodkin A. N., Simeonidis E., Balling R., Westerhoff H. V. Computing life: Add logos to biology and bios to physics. Progress in Biophysics & Molecular Biology. 2012, 111(2-3), 69—74, DOI: 10.1016/j.pbiomolbio.2012.10.003.
- Kolodkin A. N., Bruggeman F. J., Plant N., Mone M. J., Bakker B. M., Campbell M. J., et al. Design principles of nuclear receptor signaling: how complex networking improves signal transduction. Mol. Syst. Biol. 2010, 6, 446, DOI: 10.1038/msb.2010.102.
- Kolodkin A. N., Simeonidis E., Balling R., Westerhoff H. V. Understanding complexity in neurodegenerative diseases: in silico reconstruction of emergence. Frontiers in Systems Physiology. 2012, 3, 291, DOI: 10.3389/fphys.2012.00291.
- Wall M. E., Hlavacek W. S., Savageau M. A. Design of gene circuits: Lessons from bacteria. Nature Reviews Genetics. 2004, 5(1), 34—42, DOI: 10.1038/nrg1244.
- Wouters A. G. Design explanation: Determining the constraints on what can be alive. Erkenntnis. 2007, 67(1), 65—80, DOI: 10.1007/s10670-007-9045-2.
- Behe M. J. Darwin’s black box : the biochemical challenge to evolution. Free Press: New York. 2006, ISBN 0684834936.
- Анохин П. К. Очерки по физиологии функциональных систем. Медицина: Москва. 1975, ISBN 978-5-458-38439-11975.
- Heidemann D. (Ed.). Teleology. Kant Yearbook. 2009.
- Лосев А. Ф. Собрание сочинений. Том 1. Бытие. Имя. Космос. Издательство «Мысль», Российский открытый университет: Москва. 1993, ISBN 5-244-00717-3.
- Westerhoff, H.V., Kolodkin, A. N. Advice from a systems-biology model of the corona epidemics. NPJ Syst. Biol. Appl. 2020, 6, 18, DOI: 10.1038/s41540-020-0138-8.
- Kiselev I. N., Akberdin I. R., Kolpakov F. A. Delay-differential SEIR modeling for improved modelling of infection dynamics. Sci. Rep. 2023, 13(1), 13439, DOI: 10.1038/s41598-023-40008-9.
- Emmi A., Rizzo S., Barzon L., Sandre M., Carturan E., Sinigaglia A., et al. Detection of SARS-CoV-2 viral proteins and genomic sequences in human brainstem nuclei. NPJ Parkinsons Dis. 2023, 9(1), 25, DOI: 10.1038/s41531-023-00467-3
- Kolodkin A. N., Sharma P. R, Colangelo A. M., Ignatenko A., Martorana F., Jennen D., et al. ROS networks: designs, aging, Parkinson’s disease and precision therapies. NPJ Syst. Biol. Appl. 2020, 6(1), 34, DOI: 10.1038/s41540-020-00150-w.
- Zubarev I., Vladimirtsev D., Vorontsova M., Blatov I., Shevchenko K., Zvereva S., et al. Viral Membrane Fusion Proteins and RNA Sorting Mechanisms for the Molecular Delivery by Exosomes. Cells. 2021, 10(11), 3043, DOI: 10.3390/cells10113043.
- Renz A., Widerspick L., Dräger A. FBA reveals guanylate kinase as a potential target for antiviral therapies against SARS-CoV-2 Click here to expand. Bioinformatics. 2020, 36(2), i813—i821, DOI: 10.1093/bioinformatics/btaa813.
- Ostaszewski M., Niarakis A., Mazein A., Kuperstein I., Phair R., Orta-Resendiz A.,et al. COVID-19 Disease Map community. COVID-19 Disease Map a computational repository of SARS-CoV-2 virus-host interaction mechanisms. Mol. Syst. Biol. 2021, 17(10), e10387, DOI: 10.15252/msb.202110387.
- Fischer A., Zhang L., Elbéji A., Wilmes P., Oustric P., Staub T., et al. Long COVID Symptomatology After 12 Months and Its Impact on Quality of Life According to Initial Coronavirus Disease 2019 Disease Severity. Open Forum Infect. Dis. 2022, 9(8), ofac397, DOI: 10.1093/ofid/ofac397.
- Khristichenko M., Nechepurenko Y., Grebennikov D., Bocharov G., Computation and analysis of stationary and periodic solutions of the COVID-19 infection dynamics model. Journal of Bioinformatics and Computational Biology. 2025, 23(1), 2540001, DOI: 10.1142/S0219720025400013.
- Tsurkalenko O., Bulaev D., O’Sullivan M.P., Snoeck C., Ghosh S., Kolodkin A., et al. CON-VINCE consortium and the ORCHESTRA working group. Creation of a pandemic memory by tracing COVID-19 infections and immunity in Luxembourg (CON-VINCE). BMC Infect. Dis. 2024, 24(1), 179, DOI: 10.1186/s12879-024-09055-z.
- Conde P. M., Bulaev D., Rauschenberger A., Ohnmacht J., Fritz J. V., O’Sullivan M. P., et al. Distinguishing Post COVID from Pandemic-Related Health Effects: Insights from a 4-Year Prospective Cohort Study. Journal of Infection, 2025, in press.
- Novelli S., Reinkemeyer C., Bulaev D., O’Sullivan M.P., Snoeck C., Rauschenberger A., et al. Waning of anti-SARS-CoV-2 antibodies after the first wave of the COVID-19 pandemic in 2020: a 12-month-evaluation in three population-based. PloS One. 2025, 20(5), e0320196, DOI: 10.1371/journal.pone.0320196.
- Westerhoff H. V., Brooks A. N., Simeonidis E., Garcia-Contreras R., He F., Boogerd F. C., et al. Macromolecular networks and intelligence in microorganisms. Frontiers in microbiology. 2014, 5, 379, DOI: 10.3389/fmicb.2014.00379.
- Kolodkin A., Alberghina L, Snoep J. L., Piccialli G., Borsani M., Westerhoff H. V. Infrastructure Systems Biology Europe (ISBE): Emergence of Innovative Systems Biology Servicing Abstract book of 4th Dutch Bioinformatics & Systems Biology Conference Congrescentrum De Werelt, Lunteren. 71, DOI: 10.18699/BGRSSB-2018-108.
- Dos Santos M. V., Anton M., Szomolay B., Ostaszewski M., Arts I., Benfeitas R., et al. Systems Biology in ELIXIR: modelling in the spotlight. F1000Research. 2022, 11(ELIXIR), 1265, DOI: 10.12688/f1000research.126734.1.