Оценка влияния наночастиц оксида графена на клетки линии MCF-7 под действием БИК-облучения
Evaluation of the effects of graphene oxide nanoparticles on MCF-7 cells under NIR irradiation- DOI
- 10.5922/ATB-2025-1-1-2
- Страницы / Pages
- 20-30
Аннотация
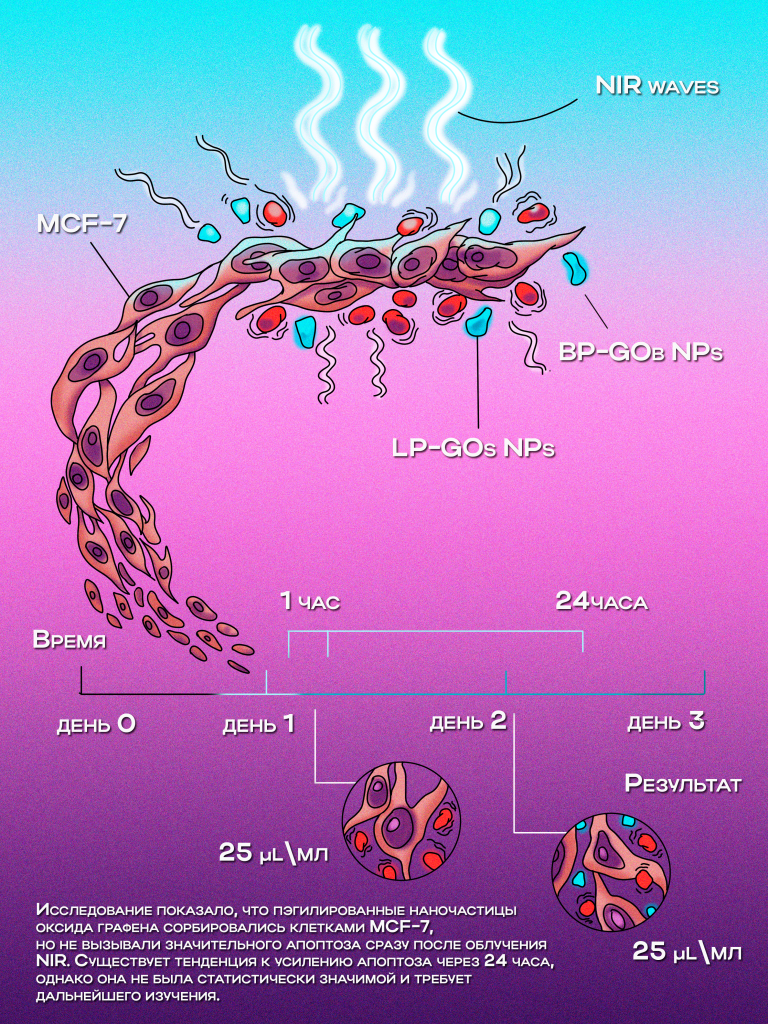
Поиск новых способов индукции апоптоза опухолевых клеток является актуальной задачей биомедицины. Учитывая уникальную теплопроводность графена, мы использовали данный наноматериал для нагрева клеток под воздействием ближнего инфракрасного излучения (БИК) в условиях in vitro. В работе применялись наночастиц оксида графена, покрытые линейным (лП-ОГм, Ø184 ± 73 нм) и 8-разветвленным (рП-ОГб, Ø1376 48 мкм) полиэтиленгликолем. Объектом исследования являлась клеточная линия аденокарциномы молочной железы MCF-7. Клетки культивировали 24 часа для образования монослоя. После этого добавляли наночастицы лП-ОГм и рП-ОГб в конечной концентрации 5 и 25 мкг/мл и затем облучали БИК-лучами (лампа Hydrosun 750) в течение 1 часа. Оценивали жизнеспособность клеток, поглощение/адгезию наночастиц клетками, а также параметры раннего и позднего апоптоза / некроза через 1 час и 24 часа после облучения.
Установлено, что клетки MCF-7 способны сорбировать наночастицы оксида графена, в том числе под действием БИК-облучения. Через 24 часа инкубации уровень PC7 + - клеток составлял 10 % (5 мкг/мл) и 50 % (25 мкг/ мл). Показано, что наночастицы под воздействием БИК-облучения не оказывают статистически значимого влияния на жизнеспособность и показатели раннего и позднего апоптоза/некроза клеток линии MCF-7. Однако через 24 часа после облучения наблюдается тенденция к увеличению этих показателей.
Abstract
The development of novel approaches to induce apoptosis in tumour cells remains a key challenge in contemporary biomedicine. Given the exceptional thermal conductivity of graphene, we employed one of its derivatives — graphene oxide (GO) — to achieve localised heating of cells under near-infrared (NIR) irradiation in vitro. In this study, graphene oxide nanoparticles coated with either linear (LP-GOs, Ø184 ± 73 nm) or branched (BP-GOb, Ø1376 ± 48 nm) polyethylene glycol were used. The MCF-7 breast adenocarcinoma cell line served as the cancer model. Cells were cultured for 24 hours to allow monolayer formation, after which LP-GOs and BP-GOb nanoparticles were added at final concentrations of 5 and 25 μg/mL. The cells were then irradiated with NIR light using a Hydrosun-750 lamp for 1 hour. Cell viability, nanoparticle sorption / uptake and the rates of early and late apoptosis / necrosis were assessed at 1 and 24 hours post-irradiation. MCF-7 cells exhibited the capacity for sorption of PEGylated graphene oxide nanoparticles, including under conditions of NIR irradiation. After 24 hours of incubation, the proportion of PC7+ (GO-positive) cells reached approximately 10 % at a concentration of 5 μg/mL and 50 % at 25 μg/mL. NIR-irradiated nanoparticles did not produce statistically significant changes in cell viability or apoptosis/necrosis rates. However, a trend towards increased cell death and apoptosis was observed 24 hours post-irradiation.
Список литературы
- Arnold M., Morgan E., Rumgay H., Mafra A., Singh D., Laversanne M., et al. Current and future burden of breast cancer: Global statistics for 2020 and 2040. Breast. 2022, 66,
- 15—23, DOI: 10.1016/j.breast.2022.08.010.
- Gao J. J., Swain S. M. Luminal A Breast Cancer and Molecular Assays: A Review. Oncologist. 2018, 23(5), 556—565, DOI: 10.1634/theoncologist.2017-0535.
- Dolgikh М. D., Zamorina S. A. The MCF-7 cell line: characteristics and interaction with nanomaterials of different structures. Bulletin of Perm University. Biology. 2024, 2, 231—247, DOI: 10.17072/1994-9952-2024-2-231-247.
- Trelles M. A., Rigau J., Sala P., Calderhead R. G., Ohshiro T. Infrared diode laser in low reactive-level laser therapy (LLLT) for knee osteoarthrosis. Laser therapy. 2005, 14, 67—71, DOI: 10.5978/islsm.91-OR-20.
- Zhu Y., Murali S., Cai W., Li X., Suk J. W., Potts J. R., et al. Graphene and graphene oxide: synthesis, properties, and applications. Adv. Mater. 2010, 22(35), 3906—3924, DOI: 10.1002/adma.201001068.
- Ding, Z., Zhang Z., Ma H., Chen Y. In Vitro Hemocompatibility and Toxic Mechanism of Graphene Oxide on Human Peripheral Blood T Lymphocytes and Serum Albumin. ACS Applied Materials & Interfaces. 2014, 6(22), 19797—19807, DOI: 10.1021/am505084s.
- Lategan K., Alghadi H., Bayati M., Fidalgo de Cortalezzi M., Pool E. Effects of Graphene Oxide Nanoparticles on the Immune System Biomarkers Produced by RAW 264.7 and Human Whole Blood Cell Cultures. Nanomaterials. 2018, 8(2), 125, DOI: 10.3390/nano8020125.
- Campos-Delgado J., Castro K. L.S., Munguia-Lopez J. G., González A. K., Mendoza M. E., Fragneaud B., et al. Effect of graphene oxide on bacteria and peripheral blood mononuclear cells. Journal of Applied Biomaterials & Functional Materials. 2016, 14(4),
e423—e430, doi:10.5301/jabfm.5000325. - Khramtsov P., Bochkova M., Timganova V., Nechaev A., Uzhviyuk S., Shardina K., et al. Interaction of Graphene Oxide Modified with Linear and Branched PEG with Monocytes Isolated from Human Blood. Nanomaterials. 2022, 12(1), 126, DOI: 10.3390/nano12010126.
- Dąbrowski B., Żuchowska A., Brzózka Z. Graphene oxide internalization into mammalian cells — a review. Colloids Surf B Biointerfaces. 2023, 221, 112998, DOI: 10.1016/j.colsurfb.2022.112998.
- Kheiltash F., Parivar K., Hayati Roodbari N., Sadeghi B., Badiei A. Effects of 8-hydroxyquinoline-coated graphene oxide on cell death and apoptosis in MCF-7 and MCF-10 breast cell lines. Iran J. Basic Med. Sci. 2020, 23(7), 871—878, DOI: 10.22038/ijbms.2020.41277.9751.
- Yang K., Zhang S., Zhang G., Sun X., Lee S. T., Liu Z. Graphene in mice: ultrahigh in vivo tumor uptake and efficient photothermal therapy. Nano Lett. 2010, 10(9), 3318—3323, DOI: 10.1021/nl100996u.
- Revuri V., Mondal J., Lee Y. K. Graphene as Photothermal Therapeutic Agents. Adv. Exp. Med. Biol. 2022, 1351, 177—200, DOI: 10.1007/978-981-16-4923-3_9.
- Li X., Wang Y., Liu T., Zhang Y., Wang C., Xie B. Ultrasmall graphene oxide for combination of enhanced chemotherapy and photothermal therapy of breast cancer. Colloids Surf. B Biointerfaces. 2023, 225, 113288, DOI: 10.1016/j.colsurfb.2023.113288.
- Ahmed K., Tabuchi Y., Kondo T. Hyperthermia: an effective strategy to induce apoptosis in cancer cells. Apoptosis. 2015, 20(11), 1411—1419, DOI: 10.1007/s10495-015-1168-3.
- Hou Y. J., Yang X. X., Liu R. Q., Zhao D., Guo C. X., Zhu A. C., et al. Pathological Mechanism of Photodynamic Therapy and Photothermal Therapy Based on Nanoparticles. Int. J. Nanomedicine. 2020, 2020, 15, 6827—6838, DOI: 10.2147/IJN.S269321.